Kardiologische Untersuchungen
Informationen über kardiologische Untersuchungen
Myokardszintigrafie
Radiopharmaka und Untersuchungsprotokolle
Die Myokardperfusionsszintigrafie wird in der klinischen Routine vorwiegend mit Tc-99m-Sestamibi durchgeführt.
Da sich Tc-99m-Sestamibi nur in vitalem Myokard anreichern, ist dieses Radiopharmaka auch zur Vitalitätsprüfung des Myokards geeignet. Die zuverlässigste nuklearmedizinische Methode zum Nachweis minderperfundierten, aber vitalen Myokards ist die Positronen-Emissions-Computertomografie (PET) mit F-18-Deoxyglukose. Sie wird derzeit als Referenzmethode für die Vitalitätsbestimmung des Myokards angesehen (Schelbert 1991).
Tc-99m-Sestamibi
Tc-99m-Sestamibi wird passiv über Diffusion in die Myokardzelle aufgenommen (Mousa et al. 1987b). Werden verschiedene aktive Transportsysteme durch Amilorid (Na/H-Austausch), g-Strophantin (Na/K-ATPase), Verapamil (Ca-Kanal) oder Bumetanid (Na/K-2Cl-Cotransport) inaktiviert, reduziert sich die Tc-99m-Sestamibiaufnahme in kultivierte Myokardzellen nicht (Piwnica-Worms et al. 1990).
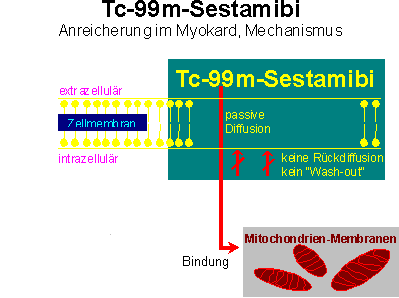
In Experimenten an kultivierten Myokardzellen konnte belegt werden, dass die Anreicherung von Tc-99m-Sestamibi durch den Zellmetabolismus beeinflusst wird, da das Membranpotential nur durch eine intakte Atmungskette bzw. einen ungehinderten Glukosemetabolismus aufrecht erhalten werden kann (Chiu et al. 1990). Zellen in Geweben wie Herz, Leber und Nieren mit einem hohen Gehalt an Mitochondrien und erhaltenem negativen Membranpotential reichern deshalb Tc-99m-Sestamibi stark in der inneren Mitochondrienmatrix an (Piwnica-Worms et al. 1989).
Es besteht eine enge Korrelation zwischen der regionalen myokardialen Perfusion und der Tc-99m-Sestamibi-Aufnahme in das Myokard (Canby et al. 1990, Mousa et al. 1990, Khaw und Mousa 1991). Tc-99m-Sestamibi reichert sich bei hohem koronaren Blutfluss (>2,5 ml/min/g) nicht mehr proportional zum myokardialen Blutfluss im Myokard an, da dann die Extraktionsfraktion sinkt (Marshall et al. 1990, Meerdink et al. 1990, Mousa et al. 1990). In minderperfundierten Myokardarealen reichert sich Tc-99m-Sestamibi im Vergleich zu Mikrosphären vermehrt an, was durch einen Anstieg der Extraktionsfraktion zu erklären ist (Li et al. 1988).
Im Myokard aufgenommenes Tc-99m-Sestamibi wird langsam wieder ausgewaschen. Nach zwei Stunden werden im linken Ventrikel noch 91%, nach sechs Stunden noch 73% der initialen Aktivität gemessen (Franceschi et al. 1990).
Die myokardiale Tc-99m-Sestamibi-Clearance in ischämischen und normal perfundierten Myokardarealen unterscheidet sich nicht signifikant (Okada et al. 1988, Glover et al. 1990, Stirner et al. 1988). Im Gegensatz zu Tl-201 unterliegt Tc-99m-Sestamibi innerhalb eines Zeitraums von vier Stunden keiner signifikanten Redistribution (Williams et al. 1986, Stirner et al. 1988, Beller et al. 1991).
Eine weitere Determinante der Tc-99m-Sestamibi-Anreicherung im Myokard ist die Vitalität des Gewebes (Liu et al. 1991). Stark hypoxisch geschädigte Myokardzellen zeigen eine verminderte Tc-99m-Sestamibi-Aufnahme (Sinusas et al. 1989, Mousa et al. 1987b), nekrotische Myokardzellen reichern kein Tc-99m-Sestamibi mehr an (Freeman et al. 1991, Boucher et al. 1990). Im Tierversuch korreliert die Größe eines Defekts im Tc-99m-Sestamibi-Myokardszintigramm gut mit der histologisch ermittelten Infarktgröße (Sinusas et al. 1990).
Die Myokardszintigrafie mit Tc-99m-Sestamibi
Die Sensitivität der Szintigrafie lässt sich mit Tc-99m-Sestamibi steigern, wenn das Radiopharmakon während einer Belastung auf dem Fahrradergometer injiziert wird. Unter Belastungsbedingungen wie bei der Fahrradergometrie oder der Vasodilatation mit Dipyridamol steigt mit der Zunahme des koronaren Blutflusses die Tc-99m-Sestamibi-Anreicherung im Myokard an (Savi et al. 1989, Mousa et al. 1990, Taillefer 1990). Eine verminderte Anreicherung wird als belastungsbedingte Ischämie bei verminderter koronarer Perfusionsreserve interpretiert (Stirner et al. 1988, Büll et al. 1990b). Tc-99m-Sestamibi zeigt keine Redistribution im Myokard (Stirner et al. 1988, Beller et al. 1991). Wegen der fehlenden Redistribution ist nach der Belastungsaufnahme eine zweite Tc-99m-Sestamibi-Injektion erforderlich, um wie mit Tl-201 Ischämiegebiete erkennen zu können (Franceschi et al. 1990, Taillefer 1990, Stirner et al. 1988). Sie sollte nach weitgehendem Abklingen der Restaktivität im Myokard erfolgen. Ist das Zeitintervall zwischen beiden Injektionen kürzer als 48 Stunden, muss die Aktivität der zweiten Injektion wesentlich höher gewählt werden als die der ersten (Picard et al. 1988). Ein reversibler, sich in der Ruhephase auffüllender Defekt korreliert mit einer relativen Minderperfusion bis hin zur belastungsinduzierten Ischämie (Larock et al. 1990).
In Kenntnis der Verteilung des Tc-99m-Sestamibi in den interessierenden Organen empfehlen Savi et al. (1989), die Datenakquisition 0,5 bis zwei Stunden nach der Injektion unter Belastung und eine bis zwei Stunden nach der Injektion in Ruhe durchzuführen.
Die Tc-99m-Sestamibi-Untersuchungsprotokolle
Da wegen nur geringer Redistribution des Tc-99m-Sestamibi getrennte Injektionen unter Belastung und in Ruhe erforderlich sind, können verschiedene Untersuchungsprotokolle eingesetzt werden. Die Untersuchung erfolgt entweder als Zwei-Tagesprotokoll, wobei mit der Szintigrafie in Ruhe oder nach Belastung begonnen werden kann. Dabei werden in beiden Untersuchungen etwa 370 MBq Tc-99m-Sestamibi injiziert (Berman et al. 1994).
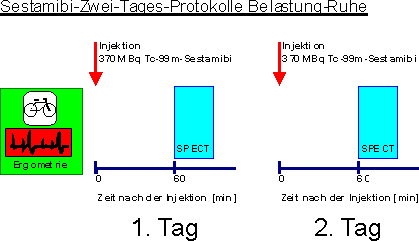
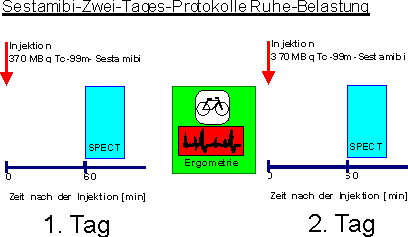
Alternativ können die Ruhe- und Belastungsaufnahme ohne Sensitivitäts- oder Spezifitätsverlust in einem Ein-Tagesprotokoll am selben Tag angefertigt werden. Wie beim Zwei-Tagesprotokoll kann sowohl mit der Untersuchung unter Belastung als auch in Ruhe begonnen werden. Bei der ersten Untersuchung werden 185 MBq, bei der zweiten 555 MBq Tc-99m-Sestamibi intravenös injiziert. Da zur zweiten Untersuchung die dreifache Aktivitätsmenge injiziert wird, ist der Einfluss der aus der Erstuntersuchung im Myokard verbliebenen Restaktivität auf die Bildgebung gering. Die Aufnahmen werden jeweils eine Stunde nach der Tc-99m-Sestamibi-Injektion angefertigt (Berman et al. 1994).
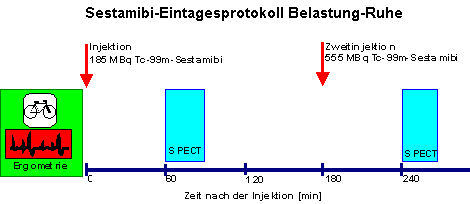
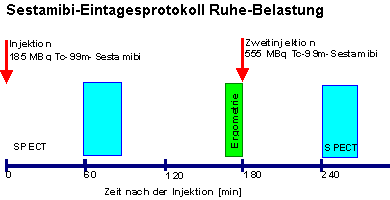
Im Vergleich zwischen am selben Tag und an zwei verschiedenen Tagen angefertigten Belastungs- und Ruheaufnahmen ließen sich keine signifikanten Unterschiede feststellen (Berman et al. 1994, Borges Neto et al. 1990, Büll et al. 1990a, Taillefer et al. 1988c). Bei einem Abstand zwischen beiden Injektionen von weniger als zwei Stunden sollte die Injektion in Ruhe vor der Injektion unter Belastung erfolgen, da die Restaktivität im Myokard nach Injektion in Ruhe geringer ist als unter Belastung (Taillefer et al. 1989a, Taillefer 1990). Beträgt das Zeitintervall zwischen beiden Injektionen drei Stunden oder mehr, lassen sich unabhängig von der Reihenfolge der Injektionen gleich gute Ergebnisse erzielen (Mohammed et al. 1990, Heo et al. 1992).
Der Vorteil der Zwei-Tagesprotokolle liegt darin, dass sich bei minimaler Untergrundaktivität Perfusionsdefekte im Szintigramm mit optimalem Kontrast darstellen (Berman et al. 1994).
Der Vorteil der Ein-Tagesprotokolle liegt darin, dass das Untersuchungsergebnis früher vorliegt und die Dauer des stationären Aufenthalts dadurch verkürzt werden kann. Ein Nachteil liegt darin, dass in der Zweituntersuchung die Restaktivität der Erstuntersuchung miterfasst wird. Eine Beurteilung der Myokardvitalität kann dadurch erschwert werden. Wird im Ein-Tagesprotokoll mit der Szintigrafie in Ruhe begonnen, muss damit gerechnet werden, dass ein Perfusionsdefekt im Belastungsszintigramm kontrastärmer dargestellt wird, da die Restaktivität eine belastungsinduzierte Minderanreicherung kompensieren kann (Whalley et al. 1991). Dieser Nachteil kann behoben werden, wenn die Untersuchung mit der Szintigrafie nach Belastung begonnen wird. Auch kann bei einem vollkommen unauffälligen Belastungsszintigramm auf eine Untersuchung in Ruhe verzichtet werden (Leppo 1991).